
海洋来源生物碱Cyanogramide生物合成机制研究取得重要进展
近日,国际著名期刊Angewandte Chemie International Edition(《德国应用化学》)在线发表了由中国科学院南海海洋研究所张长生研究员团队和中国海洋大学朱伟明教授合作的研究论文“Refactoring the Concise Biosynthetic Pathway of Cyanogramide Unveils Spirooxindole Formation Catalyzed by a P450 Enzyme”,揭示了海洋放线菌来源生物碱cyanogramide生物合成途径的重组激活和P450氧化酶催化形成氧化吲哚螺环的新机制。
生物碱cyanogramide(1)分离自海洋来源稀有放线菌Actinoalloteichus cyanogriseus WH1-2216-6,含有罕见的氧化吲哚螺[3,4]吡咯[1,2-c]并咪唑结构,可有效逆转肿瘤细胞株耐药性,如阿霉素(adriamycin)抗性细胞株K562/A02,MCF-7/Adr和长春新碱(vincristine)抗性细胞株KB/VCR。野生菌株中1的产量极低,限制了对其进行更广泛的生物活性评估和深入研发。微生物次级代谢产物生物合成研究是发现新颖合成机制、提高产量和增加结构多样性的有效途径。研究人员通过合成生物学技术手段,在异源宿主Streptomyces coelicolor YF11中重构了1的生物合成基因簇,成功实现了1的异源表达,与野生型相比,1的产量显著提高。同时,从异源表达菌中分离鉴定了9个结构类似物,包括5个新化合物cyanogramide B-D(4-6),marinacarbolines E-F(3,8)。进一步研究发现,化合物4为外消旋体,化合物5、6和1是对映异构体混合物,比例分别是5a/5b为4:1,6a/6b为5:1,1a/1b为8:1,其中,6a的绝对构型通过单晶衍射确定为12S。经过系统的基因缺失、次级代谢中间体分离鉴定和前体喂养实验,阐明了cyanogramide的生物合成途径(图1)。
氧化吲哚螺环结构单元在天然产物中广泛存在,是活性化合物中重要的药效基团,但其生物合成机制仅在真菌中有过报道。目前已报道的氧化吲哚螺环催化机制有两种,一类是通过环氧中间体,经半频哪醇重排反应产成,由黄素蛋白催化;一类是通过自由基产生,由P450氧化酶催化。研究人员发现,与真菌450氧化酶通过自由基机制生成氧化吲哚螺环不同,化合物1中的氧化吲哚螺环是由P450通过碳正离子介导的半频哪醇重排(semipinacol-type rearrangement)反应形成(图2)。这个新机制的发现拓展了P450氧化酶催化功能的认知。
中国科学院南海海洋研究所朱义广研究员和张庆波副研究员为论文共同第一作者,研究工作得到青岛海洋科学与技术试点国家实验室开放课题、国家自然科学基金项目、国家重点研发计划项目和中国科学院战略性先导科技专项等项目的资助。
相关论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202004978
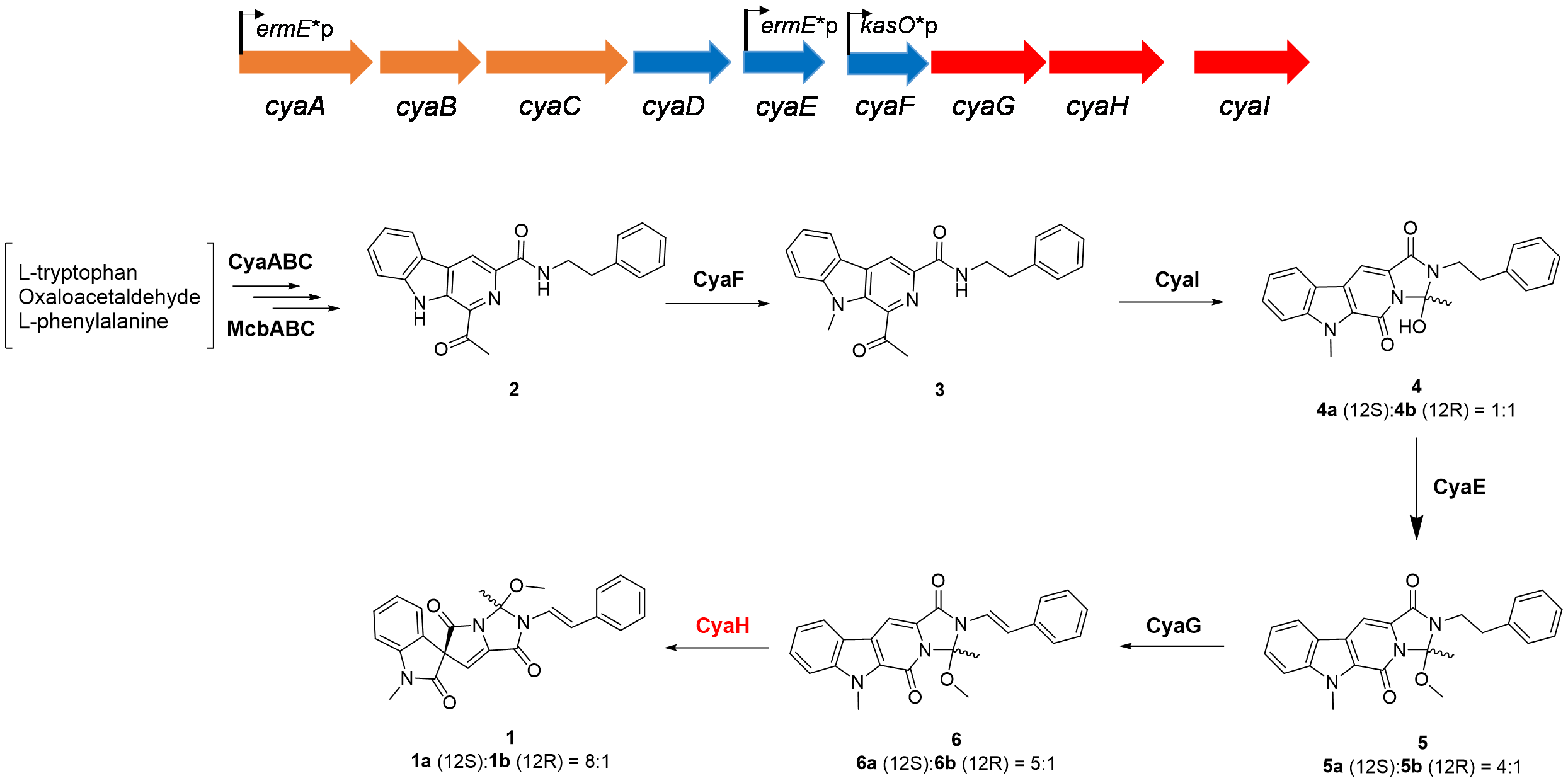
图1. Cyanogramide生物合成基因簇和推导的生物合成途径
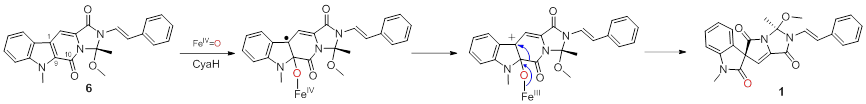
图2. 推导的CyaH催化氧化吲哚螺环形成机理