
深圳先进院等研发出循环肿瘤/融合细胞无标记分选的新型微流控技术
近日,中国科学院深圳先进技术研究院(简称“深圳先进院”)医工所微纳中心的陈艳团队在肿瘤液体活检领域取得重要进展,研发了一种创新的微流控技术,能够同时分选癌症患者外周血中的循环肿瘤细胞(Circulating tumor cells, CTCs)和循环融合细胞(Circulating fusion cells, CFCs),可以一步式从全血样品中分离出高纯度、高活性的CTCs和CFCs,并完成高通量单细胞转录组测序分析。相关研究成果以Cascaded filter deterministic lateral displacement microchips for isolation and molecular analysis of circulating tumor cells and fusion cells为题发表在微流控领域顶尖期刊Lab on a Chip上。深圳市瑞格生物科技的刘宗彬博士、深圳市第二人民医院的刘爱学主任、深圳先进院的陈艳研究员为论文的共同通讯作者。
一个世纪以前,德国病理学家Otto Aichel发现肿瘤细胞可以和免疫细胞融合,形成的融合细胞同时具备免疫细胞运动能力和肿瘤细胞的成瘤能力,更容易通过循环系统在体内扩散转移,但由于技术手段的限制,这类融合细胞很难分选出来,无法做更深入的分析。
在本研究中,研究人员提出“过滤式确定性侧向位移”(filter-DLD)的创新概念,通过微纳结构设计和有限元多物理场分析,构建了一种流体力学新结构,可实现细胞运动轨迹精准操控。这种结构不但比传统设计具有更低的临界细胞分离尺寸,而且对血液中占比最多的红细胞有极好的过滤效果。研究人员同时利用创新的流体力学结构,将filter-DLD结构整合成高度集成的级联式芯片(CFD-Chip),一方面大大提升了样品分离的通量,另一方面通过不同微结构的组合实现CTCs和CFCs的高效分选:捕获效率>96%,极高的纯度 (白细胞去除率99.995%),高活性(>98%)。因此,CFD-chip在循环稀有细胞的分选中展示出极其优越的性能。微流控芯片无标记分选的便捷流程以及全血样本的处理模式,为肿瘤液体活检的临床推广提供了科研利器。
研究人员使用CFD-Chip分析了近百例临床肺癌患者的样本,高效收集了CTCs,并鉴定了一种新的CTC亚群:肿瘤细胞-白细胞融合细胞(CFCs),CFCs同时表达肿瘤细胞和白细胞marker。患者样品中CTCs水平的变化,可以有效地应用于治疗效果的评估和病情的动态监测。由于从CFD-Chip平台获取的肿瘤细胞具有极高的活性,可以直接用高通量单细胞RNA测序进行下游分析,结果显示肺癌病人外周血中存在比CTCs数量更多的CFCs细胞。CFCs有望揭示肿瘤演化和转移的新机制,为肿瘤早期诊断、预后判断、疗效监控、复发预测提供一种新型标志物。
该研究工作得到了国家自然科学基金、中科院青年创新促进会和广东省、深圳市等科技项目的资助。
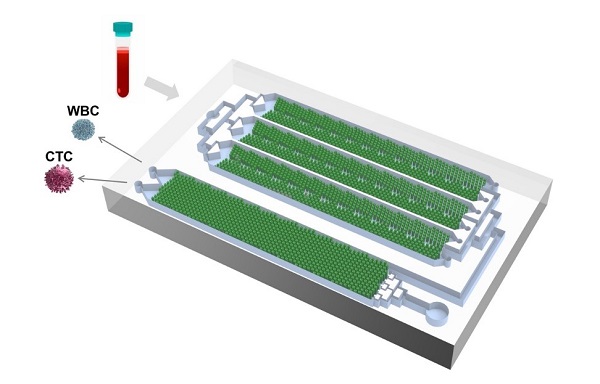
应用于循环肿瘤/融合细胞无标记分选的微流控芯片