
深圳先进院纳米材料精准生物靶向机制研究取得重要进展
8月5日,中国科学院深圳先进技术研究院纳米医疗技术研究中心李红昌课题组,联合材料界面研究中心喻学锋课题组和高分子药物研究中心李洋课题组,发现纳米材料精准生物分子靶向的新机制,相关成果以Intrinsic Bioactivity of Black Phosphorus Nanomaterials on Mitotic Centrosome Destabilization through Suppression of PLK1 Kinase为题发表在《自然—纳米技术》。李红昌课题组副研究员邵喜明和研究助理丁智昊为论文并列第一作者,李红昌研究员、喻学锋研究员和李洋副研究员为论文共同通讯作者,深圳先进院为唯一的第一和通讯作者单位。
研究团队选取黑磷纳米材料为研究对象,通过精细的细胞生物学和分子生物学研究,发现纳米材料在细胞内可通过精准靶向某个具体生物分子,以获得特定的生物效应。因此,本研究提供了一个从分子细胞生物学维度,深入研究纳米材料精准生物靶向机制的全新范例。
多年来,纳米技术一直被视为一门拥有无限潜力的科学。伴随着纳米科学技术在各行各业的普遍应用,理解纳米生物效应与安全性变得愈加重要,但相关研究却始终处于早期阶段。纳米生物作用可具有正向效应和负向效应。正向纳米生物效应,可以被用于开发新的纳米药物,将给疾病诊断和治疗带来新的机遇;而负向纳米生物效应,则会对人体、生物乃至整个生态环境产生毒性,将造成严重的生物安全隐患。因此,研究纳米材料与生物系统,特别是在细胞和分子层面的作用机理,对纳米技术的正确应用至关重要。
本研究发现使用低浓度黑磷纳米材料处理细胞,能够导致细胞分裂特异停滞在细胞周期的有丝分裂M期。整个细胞周期分为四个时期,每次分裂都严格按照G1,S,G2,M的顺序进行,其中每个过程都受到众多信号通路的精细调控。黑磷纳米材料导致细胞周期停滞在细胞周期中时程最短的M期,意味着纳米材料对M期的某个关键细胞器或某条关键信号通路功能进行了特异干扰,因此非常可能是一种材料特异的纳米生物学效应。随后,团队对这一现象背后的机理进行了深入挖掘,发现黑磷纳米材料造成有丝分裂核心细胞器---中心体(centrosome)的分离受到阻滞。这一机制被最终确定为黑磷纳米材料导致细胞分裂M期停滞的直接原因。
黑磷纳米材料导致的细胞周期阻断效应可以完全媲美于已经发现的靶向细胞分裂M期的特异小分子药物,因此团队进一步探索了黑磷纳米材料是否有特定的生物靶向分子。通过一系列生物化学和细胞生物学研究,团队最后确认有丝分裂激酶PLK1是黑磷纳米材料的生物效应靶点。黑磷纳米材料可以特异结合PLK1,并抑制其激酶活性,从而阻断了细胞分裂M期的正常进行。
抑制细胞周期是理想的抗肿瘤策略。黑磷纳米材料作为一种新型PLK1抑制剂,在实验动物模型中展现出了优秀的肿瘤抑制效果。因此假以时日,黑磷纳米材料非常有可能发展成为一个临床可用的抗肿瘤纳米药物。最重要的,本项目研究结果明确展示了纳米材料能够通过精准靶向特定生物分子进而获得特异的纳米生物学效应,因此必将带动纳米领域对不同纳米材料的内在生物学效应和分子细胞机制进行广泛研究,最终为纳米药物的研发开辟全新路径。
该研究得到了国家自然科学基金,广东省自然科学基金以及深圳市重点研究项目的支持。
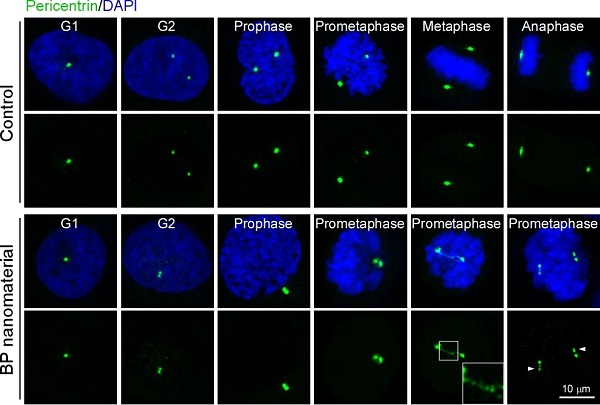
图1:细胞有丝分裂过程中,遗传物质的精准分配起始于纺锤体核心器件---中心体的正确分离。黑磷纳米材料进入分裂期细胞后,通过靶向并抑制中心体的分离,导致细胞分裂被阻断在分裂早期。
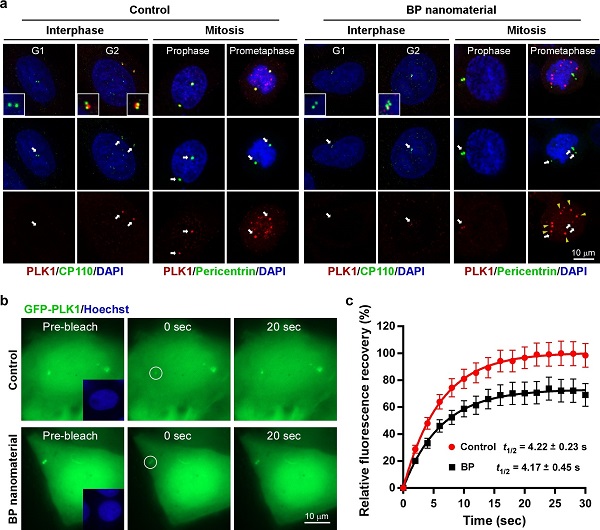
图2:PLK1是控制中心体正确分离的关键激酶,黑磷纳米材料在细胞内能够与PLK1蛋白结合,促进其异常聚集,导致PLK1无法被有效募集到中心体位置进行活化,最终影响了中心体的正常分离。a,黑磷纳米材料处理细胞减弱了PLK1在中心体的定位。b-c,黑磷纳米材料明显减缓了PLK1向中心体的动态募集。
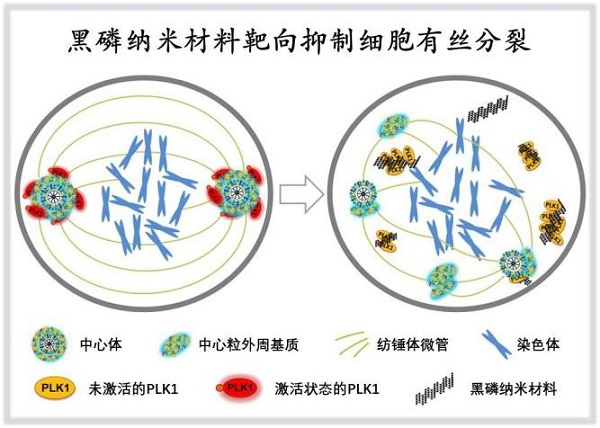
图3:黑磷纳米材料抑制细胞有丝分裂进行的分子细胞机制:黑磷纳米材料通过靶向细胞分裂关键激酶PLK1,抑制其向中心体位置的转移和活化,造成中心体正常分离被抑制,并引发中心体碎片化,进而导致多极纺锤体形成,最终抑制了细胞有丝分裂的完成。